LABORATORIO DE SEPARACIÓN DE MEZCLAS
GRADO UNDÉCIMO
INTRODUCCIÓN
Las sustancias puras se caracterizan porque tienen una composición fija y no pueden separarse por métodos físicos en otras sustancias más simples. Las mezclas o sistemas materiales se clasifican en heterogéneas cuando constan de dos o más fases y sus componentes pueden identificarse a simple vista o con ayuda de un microscopio. Las homogéneas son las llamadas comúnmente soluciones, en las que se observa una sola fase en la que todas las propiedades químicas y físicas son idénticas.
Para la separación de mezclas en el laboratorio se emplean distintos métodos que dependen de las características de la mezcla a separar, ya que presentan particularidades propias que no pueden ser separadas con cualquier elemento.
JUSTIFICACIÓN
Teniendo en cuenta el avance tanto técnico como cultural en el desarrollo de la humanidad, vemos que es de suma importancia tener presente diversos conocimientos referentes a la ciencia, en nuestro caso en la química.
Actualmente hacemos uso de métodos de separación de mezclas, en un ámbito familiar obviamente, pero de lo cual necesitamos tener un mínimo conocimiento para efectuarlas. Desde la tamizar o "colar" el arroz , hasta eliminar el agua que ha caído en el aceite.
OBJETIVOS
OBJETIVO GENERAL
Reconocer y definir los diversos métodos de separación de mezclas teniendo en cuenta el tipo de mezcla y/o sustancia.
OBJETIVO ESPECIFICO
- Reconocer los métodos de separación de mezclas teniendo en cuenta sus características
-Hacer uso en la cotidianidad de dichos métodos
MARCO TEÓRICO
Una mezcla es un sistema material formado por dos o más componentes unidos, pero no combinados químicamente. En una mezcla no ocurre una reacción química y cada uno de sus componentes mantiene su identidad y propiedades químicas. No obstante, algunas mezclas pueden ser reactivas, es decir, que sus componentes pueden reaccionar entre sí en determinadas condiciones ambientales, como una mezcla aire-combustible en un motor de combustión interna.
Es la combinación física de dos o más sustancias que retienen sus identidades y que se mezclan pudiendo formar según sea el caso aleaciones, soluciones, suspensiones y coloides.
Las mezclas se clasifican en:
-Homogéneas.
-Heterogéneas.
MEZCLA HOMOGÉNEA : son totalmente uniformes (no presentan discontinuidades al ultramicroscopio) y presentan iguales propiedades y composición en todo el sistema, algunos ejemplos son la salmuera, el aire. Estas mezclas homogéneas se denominan soluciones.
MEZCLA HETEROGÉNEA : no son uniformes; en algunos casos, puede observarse la discontinuidad a simple vista (sal y carbón, por ejemplo); en otros casos, debe usarse una mayor resolución para observar la discontinuidad.
Los componentes de una mezcla pueden ser:
-Sólidos
-Líquidos
-Gaseosos
MÉTODOS DE SEPARACIÓN DE MEZCLAS
VIDEO DEMOSTRATIVO
Para separar las mezclas en sus componentes puros, se utilizan diversas técnicas de separación, las cuales mantienen inalteradas las propiedades químicas y físicas. A continuación se describirán las técnicas más utilizadas para este propósito:
MÉTODOS
Destilación
Este método consiste en separar dos o más líquidos de una mezcla homogénea aprovechando las diferencias en los puntos de ebullición de cada uno. El proceso de la destilación consta de dos fases: la primera en la cual el líquido pasa a vapor (gas), y la segunda en la cual el vapor se condensa y pasa nuevamente a líquido. Cabe mencionar que un compuesto de punto de ebullición bajo se considera volátil en relación con los otros componentes que tienen puntos de ebullición mayor.En muchos casos al tratar de separar un componente de la mezcla por destilación en la fase gas se forma una especie de asociación entre las moléculas llamada azeótropo el cual puede presentar un cambio en el punto de ebullición al realizar la destilación. Los tipos de destilación más comunes son: destilación simple, destilación fraccionada y destilación por arrastre con vapor. En la destilación simple, el proceso consta de una sola etapa; es decir, que se evapora el líquido de punto de ebullición más bajo (mayor presión de vapor) y se condensa por medio de un refrigerante.
Evaporación
Es un proceso físico que consiste en la separación de una mezcla homogénea de un sólido disuelto en un líquido, por calentamiento, hasta que el líquido hierve y se transforma en vapor. Como no todas las sustancias se evaporan con la misma rapidez, el sólido disuelto se obtiene en forma pura.
Por ejemplo, si a un vaso que contenga una solución acuosa de sulfato de sodio se le aplica calor, al cabo de un tiempo el agua se evaporará y el componente sólido de la mezcla, el sulfato de sodio, quedará en el fondo del vaso.
Cristalización
Este método se utiliza para purificar (eliminar contaminantes) una sustancia sólida. Para ello, se disuelve el sólido en un solvente caliente en el cual los contaminantes no sean solubles; luego se filtra en caliente para eliminar las impurezas y después se deja enfriar el líquido lentamente hasta que se formen los cristales.
Los cristales pueden formarse de tres maneras:
Por fusión: para cristalizar una sustancia como el azufre por este procedimiento, se coloca el azufre en un crisol y se funde por calentamiento, se enfría y cuando se ha formado una costra en la superficie, se hace un agujero en ella y se invierte bruscamente el crisol, vertiendo el líquido que queda dentro. Se observará una hermosa malla de cristales en el interior del crisol.
Por disolución: Consiste en saturar un líquido o disolvente, por medio de un sólido o soluto y dejar que se vaya evaporando lentamente, hasta que se han formado los cristales.
También puede hacerse una disolución concentrada en caliente y dejarla enfriar. Si el enfriamiento es rápido, se obtendrán cristales pequeños, y si es lento, cristales grandes.
Sublimación: Es el paso directo de un sólido a gas, como sucede con el Iodo y la naftalina al ser calentados, ya que al enfriarse los gases originan la cristalización por enfriamiento rápido.
Cromatografia
Es un poderoso método de separación de mezclas que tiene aplicación en las diferentes áreas de la ciencia. En todas las separaciones cromatográfícas, la muestra se desplaza a diferente velocidad con una fase móvil, que puede ser un gas, un líquido, etc. Esta fase móvil se hace pasar a través de una fase estacionaria o medio adsorbente, con la que es inmiscible, y que se fija a una columna o a una superficie sólida. Las dos fases son elegidas selectivamente, de modo que los componentes de la muestra se distribuyen diferente entre la fase móvil y la fase estacionaria. Aquellos compuestos que se retienen mayormente a la fase estacionaria o columna, se desplazan lentamente. Mientras que los compuestos que son débilmente retenidos por la columna fluyen en conjunto con la fase móvil. Como consecuencia del diferente desplazamiento (rápido o lento), los componentes de la mezcla se separan en bandas o zonas discretas que pueden analizarse cualitativamente y/o cuantitativamente.En términos simples podemos definir a la cromatografía como un método físico de separación en el cual los componentes de la mezcla que se han de separar se distribuyen entre dos fases, una en reposo (fase estacionaria) y la otra en movimiento, que se desplaza a una dirección definida (fase móvil). La figura 1 se ilustra la cromatografía en papel, donde se aprecia la fase estacionaria (papel) y la fase móvil es un líquido (alcohol) que fluye a través de esta, separando la mezcla que se deposita en la parte inferior.
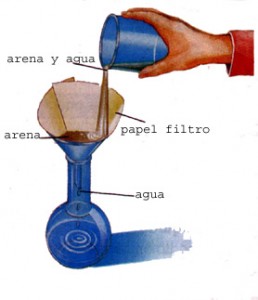
Filtración
Este método sirve especialmente para separar sólidos insolubles de grano fino que forman una mezcla heterogénea con el líquido.
Consiste en verter la mezcla a través de un medio poroso que deje pasar el líquido y retenga el sólido. Por ejemplo, una mezcla heterogénea de leche con harina se puede filtrar para separar sus fases.
Los aparatos usados se llaman filtros; el más común es el de porcelana porosa, usado en los hogares para purificar el agua. Los medios más porosos más usados son: el papel filtro, la fibra de vidrio o asbesto, telas etc.
En el laboratorio se usa el papel filtro, que se coloca en forma de cono en un embudo de vidrio, a través del cual se hace pasar la mezcla, reteniendo el filtro la parte sólida y dejando pasar el líquido.
Tamizado o cribado
Consiste en separar una mezcla heterogénea de materiales sólidos de tamaños diferentes; por ejemplo, granos de caraota (judías, alubias, frijoles o porotos, según el país) y arena empleando un tamiz (colador).
Los granos de arena pasan a través del tamiz y los granos de la leguminosa quedan retenidos.
Imantación o separación por magnetismo
Consiste en separar con un imán los componentes de una mezcla heterogénea formada por un elemento metálico y otro no metálico. Por ejemplo, al acercar un imán a una mezcla de hierro y azufre, el hierro es atraído hacia el imán logrando separarse del azufre.
Centrifugación
Método utilizado para separar mezclas heterogéneas de líquidos y sólidos haciéndolos girar a gran velocidad. Se coloca la mezcla en un tubo de ensayo que se instala en una centrífuga y se hace girar a gran velocidad: la sustancia más densa queda en el fondo y la de menor densidad, en la superficie.
Este proceso es de gran utilidad en los análisis de leche (para separar sus componentes) y sangre (para separar el plasma, el suero, etc.)
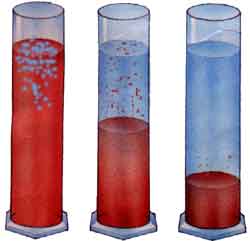
Decantación
El procedimiento de decantación consiste en separar componentes que contienen diferentes fases (por ejemplo, dos líquidos que no se mezclan, un sólido insoluble y un líquido, etcétera) siempre y cuando exista una diferencia significativa entre las densidades de las fases.
Como vemos, el método funciona mediante la diferencia de pesos, por lo que el de mayor peso se precipitará hacia el fondo como, por ejemplo, cuando se mezclan el agua y el azúcar. Después de cierto tiempo de estar mezcladas, el azúcar se va depositando en el fondo del recipiente, esto por que de las dos sustancias, es la que tiene mayor peso.
Si tenemos una mezcla de un sólido y un líquido que no disuelve dicho sólido, se deja reposar la mezcla y el sólido va al fondo del recipiente.
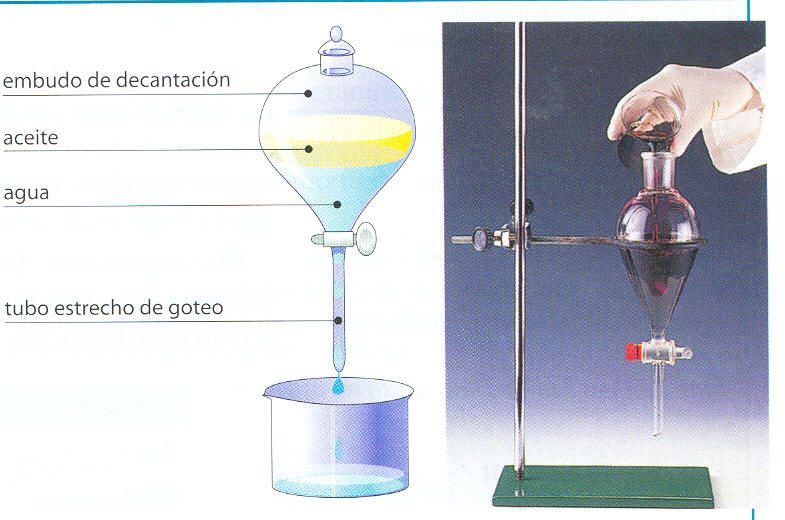
Si se trata de dos líquidos, se coloca la mezcla en un embudo de decantación, se deja reposar y el líquido más denso queda en la parte inferior del embudo.
ELEMENTOS UTILIZADOS EN LA SEPARACIÓN DE MEZCLAS
Dentro del laboratorio de química podemos encontrar una amplia gama de instrumentos o herramientas que se conocen como material de laboratorio. Estos instrumentos se usan para medir y mezclar o combinar elementos químicos.
Estos materiales se pueden clasificar tomando en cuenta dos criterios: según el material del que están hechos y por su función. Según el material pueden ser de metal, de vidrio, de madera, de goma, de porcelana o de plástico. Según su función pueden ser material volumétrico o agitadores magnéticos.
Cápsula de Porcelana: Se utiliza para calentar y evaporar líquidos y también para fundir y cristalizar sólidos. Es una cápsula convexa de porcelana ya que este es uno de los elementos mas resistentes
Estos materiales se pueden clasificar tomando en cuenta dos criterios: según el material del que están hechos y por su función. Según el material pueden ser de metal, de vidrio, de madera, de goma, de porcelana o de plástico. Según su función pueden ser material volumétrico o agitadores magnéticos.
Cápsula de Porcelana: Se utiliza para calentar y evaporar líquidos y también para fundir y cristalizar sólidos. Es una cápsula convexa de porcelana ya que este es uno de los elementos mas resistentes
- Matraz Erlenmeyer: Es un frasco cónico de vidrio de base ancha y alargada con un cuello estrecho que se usa para medir y calentar sustancias y gracias a su cuello estrecho se evita la pérdida de sustancias.
- Matraz Aforado: Es un recipiente con forma de pera, fondo plano y un cuello largo y delgado que se usa para hacer mediciones precisas y que necesiten un margen de error mínimo.
- Probeta: Es un tubo transparente y alargado que tiene una graduación que indica diferentes volúmenes. Es cerrado en la parte de abajo y tiene una base que se usa como apoyo.
- Bureta: Es un tubo largo con una graduación para medir volúmenes y en su parte inferior tiene una llave que ayuda a cumplir la función de vertir cantidades variables de liquido.
- Pipeta: Es un tubo hueco y transparente que en una de sus puntas tiene forma cónica y presenta una graduación que indica diferentes volúmenes. Sirve para medir cantidades de liquido con una presicion casi exacta.
- Tubo de ensayo: Es un tubo de vidrio con una punta abierta y la otra cerrada y redonda, que se utiliza para contener pequeñas muestras líquidas
- Cristalizador: Es un recipiente de vidrio de base ancha y poca estatura que se usa para cristalizar el soluto de una solución por evaporación del solvente.
- Mechero: Es un instrumento utilizado en laboratorios científicos para calentar o esterilizar muestras.
LABORATORIO VIRTUAL REALIZADO EN CLASE
En clase se desarrollo un laboratorio virtual, en el cual se desarrollaron diversos métodos de separación de mezclas, empleando situaciones básicas que ocurren en el hogar, entre ellas se encontraron:
WEBGRAFIA





















y las conclusiones?4.7
ResponderEliminarfijate que en el marco teorico pones que una mezcla homogenea se distingue a simple vista y esta mal.
ResponderEliminarMuy buena la ilustración cabe destacar que los experimentos de los laboratorios no son nda comunes, en este caso vengo con una sugerencia a ver si la acepta, y es que me gustaria que explicaran sobre de como hacer un caleidoscopio ya que con lo leído y muy bien explicado pienso que me pueden dar una mejor idea de como hacer esos pasos. Que le parece ?
ResponderEliminar